Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (12): 1949-1956.doi: 10.3969/j.issn.2095-4344.2551
Previous Articles Next Articles
Locking plate in the treatment of proximal humeral fractures involving humeral calcar: effective support, complications and functional recovery
Xu Peng1, 2, Su Ping3, Li Xuedong1, 2, Rui Yongjun2
- 1Soochow University, Suzhou 215008, Jiangsu Province, China; 2Wuxi No. 9 Hospital Affiliated to Soochow University, Wuxi 214000, Jiangsu Province, China; 3Department of Pathology and Pathophysiology, School of Basic Medicine, Xiamen Medical College, Xiamen 361000, Fujian Province, China
-
Received:2019-09-26Revised:2019-09-28Accepted:2019-10-31Online:2020-04-28Published:2020-03-03 -
Contact:Rui Yongjun, MD, Chief physician, Wuxi No. 9 Hospital Affiliated to Soochow University, Wuxi 214000, Jiangsu Province, China -
About author:Xu Peng, Master candidate, Soochow University, Suzhou 215008, Jiangsu Province, China; Wuxi No. 9 Hospital Affiliated to Soochow University, Wuxi 214000, Jiangsu Province, China
CLC Number:
Cite this article
Xu Peng, Su Ping, Li Xuedong, Rui Yongjun. Locking plate in the treatment of proximal humeral fractures involving humeral calcar: effective support, complications and functional recovery[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(12): 1949-1956.
share this article
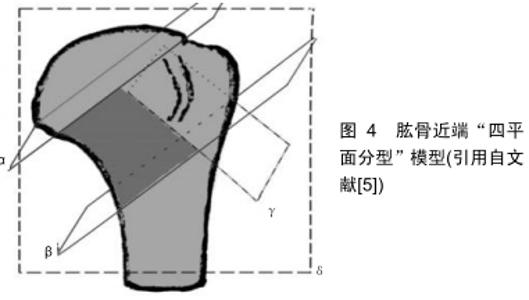
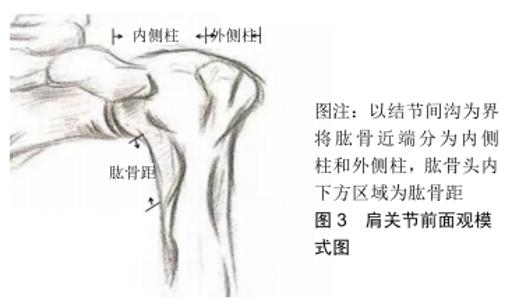
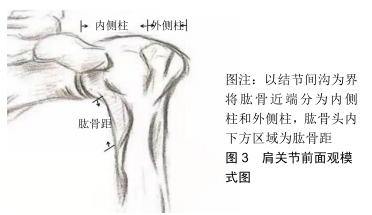
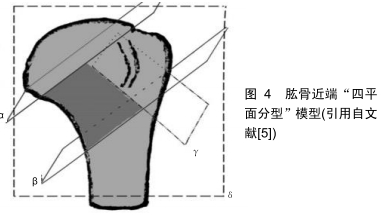
肱骨距概念的提出是为了更好地治疗肱骨近端骨折,因此理解肱骨近端肱骨距的重要性及肱骨距粉碎的形态对于治疗肱骨近端骨折非常重要。目前对肱骨距的解剖区域及肱骨距粉碎的定义没有达成统一。HASAN等[4]通过提取48例满足纳入排除标准的一级创伤中心收治的肱骨近端骨折患者的CT数据,分析骨折线地图发现,43例累及肱骨距,其中定义的肱骨距区为肱骨头以下、外科颈以上区域。2012年RUSSO等[5]通过分析100例发生肱骨近端四部分骨折的患者,总结肱骨近端四部分骨折的特征(更改部分内容),提出“四平面分型”:将“四个平面”围成的区域定义为肱骨距区域,并将累及肱骨距的骨折重新分型,把肱骨距作为除解剖颈、大结节、小结节、外科颈之外的一个特别重要的区域,将肱骨近端肱骨矩的重要性提到了重要的地位,见图4。 "

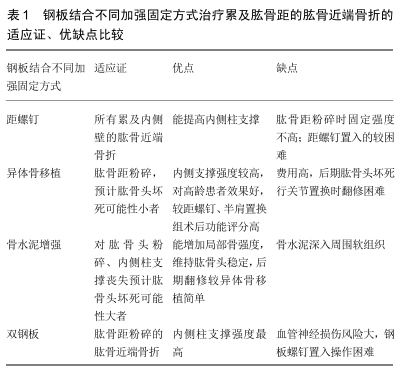
HERTEL等[6]将肱骨近端内侧矩粉碎定义为在平片上任一角度观察到内侧壁断裂并移位超过2 mm,粉碎的内侧柱将失去其力学支撑,易导致骨折块固定后不稳定并发肱骨头内翻塌陷。而OSTERHOFF等[7]则定义肱骨距粉碎为肱骨内侧解剖颈至外科颈弯曲处至少见 1个骨折块,但是大量研究肱骨距作用的生物力学实验构建的模型则是内侧壁缺损10 mm。目前尚未对肱骨距的范围及肱骨距粉碎的概念达成统一,因此统一肱骨距的解剖范围对规范肱骨距的研究很重要。 2.1.2 肱骨近端的生物力学性能 肱骨近端骨皮质厚度、密度、皮质下骨小梁密度的改变将影响整个骨的力学性能,从而易发生复杂的低能量骨折。MAJED等[8]通过软件分析37具肱骨近端标本的不同区域骨皮质厚度发现:骨皮质厚度值范围为0.33-3.5 mm,二头肌沟(最厚)、大结节(最薄),之间表现出一致的渐进性皮质变薄模式,而肱骨近端骨折线沿着皮质变薄线发生。双能X射线骨密度一直是临床工作中常常使用的指标,但是LEE等[9]提出对肱骨中央骨的双能X射线吸收测定法可能不能反映肱骨近端骨质量和预测肱骨近端骨折的严重程度。国内学者王烨明等[10]比较健康人群肱骨近端内侧壁不同区域皮质下骨小梁密度等参数发现,肱骨距区域皮质下骨小梁密度自近向远端逐渐降低,这也提示肱骨距螺钉固定时,内侧支撑螺钉应该尽量靠近内侧皮质,且螺钉长度放置至肱骨头的内下象限,这样能增加螺钉固定的强度。 2.2 肱骨距的作用及临床意义 2.2.1 肱骨距的完整性影响肱骨头血供 肱骨头的血供主要由旋肱前、后动脉供应,其中供血量最大的为旋肱后动脉支,约占肱动脉血供的64%[11],走形于肱骨头后方、上方、下方区域并供应肱骨头相应部位血供。2004年HERTEL等[6]回顾性分析100例肱骨近端囊内骨折发现,肱骨头骨块连接的肱骨内侧壁皮质长度小于8 mm、内侧铰链结构的连续性丢失、解剖颈骨折,同时满足这3个条件,肱骨头坏死的阳性预测率为97%。这些条件均提示肱骨距区域的破坏,肱骨头血供可能受到破坏。而在解剖颈劈裂,但小结节与肱骨头相连的肱骨近端骨折中,由于肱骨距结构完整,肱骨头坏死风险系数反而只有0.39,这也间接反映了内侧铰链在维持肱骨头血供中的重要性。肱骨距粉碎往往提示肱骨头、干的移位,2009年KRALINGER等[12]进行尸体研究发现,肱骨近端骨折时,肱骨头-干移位超3 mm,肱骨内侧皮质的骨膜开始撕裂;若移位大于35 mm,内侧骨膜的软组织合页作用将完全撕裂,骨膜的血供受到破坏,且当肱骨距粉碎时旋肱后动脉容易损伤。因此临床发生肱骨近端骨折伴肱骨距粉碎时,常常提示肱骨头血供受到一定程度破坏。 2.2.2 内侧壁完整性影响肩关节运动 肩关节是人体活动度最大的关节,肱骨距区域骨小梁较多也间接说明前臂力量向上传导时肱骨距受到的应力较大。冷昆鹏等[13]在体外生物力学实验中模拟肩关节外展90°,在生理状态条件对肱骨近端三维有限元模型施加600 N的轴向载荷,肱骨近端外科颈内下侧皮质区应力分布较集中,此区域应力最大值为5.2 MPa,说明内侧柱具有重要的负重作用。肱骨距区域发生骨折后对肱骨头支撑消失,力学结构发生改变,进而影响肩关节的运动。 2.2.3 肱骨距对肱骨近端骨折愈合阶段肱骨头位置起支撑、维持作用 肱骨内侧在力学上作为应力侧,对肱骨头起支撑作用。肱骨近端骨折钢板治疗最常使用Phillos钢板,钢板放在肱骨张力侧,自外向内放置的普通锁定螺钉不能为肱骨距提供支撑。2007年AGUDELO等[14]回顾性分析147例发生肱骨近端骨折患者,其中14%的术后并发症与肱骨内侧骨皮质缺损相关。肱骨内侧壁完整时肱骨距是内侧支撑的最主要结构。2007年GARDNER等[15]发现在没有获得内侧柱支撑的肱骨近端骨折病例中,29%术后发生复位丢失和螺钉穿透关节面,肱骨头的垂直高度相对于钢板下降了6 mm。为了减少肱骨钢板内固定术后内翻畸形等并发症,GARDNER等[15]首次提出使用肱骨距螺钉的概念。2013年PONCE等[16]将肱骨距粉碎与内侧壁完整2种尸体模型行钢板内固定,然后进行生物力学分析发现肱骨内侧壁粉碎可明显降低肱骨近端骨折术后稳定性,而使用距螺钉时,肱骨距粉碎模型的破坏载荷和平均破坏能量显著增加。但是学者们也发现即使肱骨距解剖复位,也有部分病例后期出现肱骨头内翻塌陷等并发症,这也提示单纯距螺钉维持肱骨近端骨折临床愈合阶段的稳定可能强度不够。2008年GARDNER等[17]又提出可以在肱骨髓腔内放置腓骨条支撑肱骨内侧柱去减少这些并发症,取得了较好的临床效果,这也提示肱骨内侧柱支撑对肱骨近端骨折愈合阶段位置的维持发挥重要作用。之后大量临床文献强调了肱骨内侧柱重建和髓腔内结构支持对结构稳定的重要性[18-19]。 2.2.4 术前预测肱骨头血供情况,术后预测肱骨头坏死发生率 营养肱骨头的血管走形经过内侧壁向肱骨头供血,所以肱骨近端骨折后骨折块移位可能影响肱骨头的血供,因此通过对肱骨内侧壁骨折形态及骨折块移位程度的判断,可以预测肱骨头血供情况。HERTEL等[6]提出肱骨头骨块连接的肱骨距内侧皮质长度可以作为肱骨头坏死预测的指标,得到广泛的认可。TRIKHA等[20]的研究也证明了肱骨距完整性及内侧皮质长度的重要性。HERTEL等[6]认为是否能用钢板重建骨折也取决于与肱骨头相连的内侧壁铰链高度,而铰链高度只能在多平面准确确定。2013年CAMPOCHIARO等[21]在Hertel的基础上,总结了267例钢板内固定治疗的肱骨近端骨折患者的肱骨头坏死情况,再次强调了内侧距的重要意义,但也提出HERTEL等[6]实验中对于肱骨距测量的不足,认为应该从多个平面的影像学进行对肱骨距的评估,术者应根据术前X射线、CT结果充分了解肱骨距骨折的形态,确定是否为“可修复性内侧壁”,通过对肱骨距的评估来确定哪些骨折是可以重建,哪些需要置换。CAI等[22]比较钢板治疗肱骨解剖颈骨折与外科颈骨折发现治疗解剖颈骨折术后更易出现肱骨头坏死等并发症,这也可以用“Hertel肱骨头血供预测”解释。虽然通过观察肱骨内侧壁骨折情况只能粗略预测肱骨头坏死率,并存在一定偏差,但是这也对医师手术方式的选择有一定参考意义。 2.2.5 肱骨近端内侧壁的复位也能减少螺钉穿出关节面、内翻畸形等并发症发生 肱骨近端内侧壁的解剖复位能恢复内侧柱的有效支撑,减少术后螺钉穿出关节面、内翻畸形等并发症。GARDNER等[15]发现内侧柱支撑在肱骨近端骨折治疗中重要性,术中未恢复内侧柱支撑的患者螺钉穿出发生率高达29%,而术中加强内侧支撑的患者螺钉穿出率仅为5.6%。BRUNNER等[23]的一项多中心前瞻性研究,通过分析157例肱骨近端骨折进行锁定钢板内固定的患者,也发现术中恢复内侧支撑将有效地降低术后螺钉穿出、内翻等并发症的发生率。HELWIG等[24]进行的前瞻性研究发现术中内侧柱能否达到解剖复位与术后螺钉穿出具有统计学上的相关性。 2.2.6 预测功能及预后 解剖复位是关节内、关节周围骨折复位的基本要求,肱骨近端内侧壁部分在关节囊内,属于关节周围骨折,因此内侧壁的解剖复位也是很重要的。CHEN等[25]发现内侧壁解剖复位、内侧柱有效支撑后患者术后功能评分较未能复位或未得到内侧支撑者明显高,功能恢复效果更好,提示内侧壁解剖复位能提高肱骨近端骨折患者术后肩关节功能。 总之,肱骨距的作用及临床意义已经越来越不容忽视,临床医生应该加强对肱骨距的认识,仔细了解内侧壁骨折的形态及移位情况,这能帮助医师术前对肱骨头血运进行评估,指导治疗方案的选择,对治疗预后的判断,一定程度能提高肱骨近端骨折的治疗效果。 2.3 内侧壁粉碎的机制及常见原因分析 2.3.1 无统一的内侧壁骨折分型标准作为指导 肱骨近端骨折目前比较认可的分型有Neer分型、Codman-Hertel分型[6]、Resch分型[26]、AO分型[27],其中AO分型与Neer分型2种较为常用。不同的分型代表着不同的骨折复杂程度,较为复杂的骨折类型意味着骨折复位难度较大,术后易发生并发症,但是AO分型及Neer分型都未描述内侧壁粉碎情况。作者检索发现仅1篇文献对四部分肱骨近端骨折内侧壁形态进行描述并分型[5],但是并未得到广泛的认可和应用,因此无统一的内侧壁分型标准也是导致临床医生对肱骨距重要性重视不够的原因。 2.3.2 X射线片显示的骨折模型与骨折实际情况不符目前大多数肱骨近端骨折的分型依据都是X射线上所显示的骨折模型,然而在一些特殊类型骨折模式下,X射线片上显示的骨折模式往往与骨折的实际情况不相符,导致了临床医师对内侧壁粉碎程度的低估。所以一般肱骨近端骨折都推荐行“创伤系列X射线片”。目前都建议术前行CT检查以明确骨折模式,甚至有学者提出3D在肱骨近端骨折中的应用[28],应用三维建模技术重建肱骨近端三、四部分骨折是可靠和准确的。这些肱骨骨折的重建结果显示,1名观察人员的组间相关系数为0.71-0.93,2名观察人员的组间相关系数为0.82-0.98,重建模型的测量结果具有良好的观察者间和观察者内可靠性。这种肱骨近端骨折的重建技术对复杂的肱骨近端骨折行切开复位内固定或半关节置换术前计划的制定大有帮助。 2.3.3 累及肱骨距的特殊骨折模式 肱骨近端骨折的分型没有一种分型将肱骨距骨折情况加入其中。但是随着肱骨距在骨折治疗选择及预后中的地位不断提高,不得不重新认识肱骨距。根据骨折的形态,肱骨距粉碎常发生Neer二、三、四部分骨折中,2002年Neer增加了一种特殊的骨折类型外翻嵌插型,对于这种类型骨折,肱骨矩通常是连续的,很少发生粉碎。HERTEL等[6]在Codman的基础上提出“二进制分型”,其中解剖颈骨折时常常伴内侧壁骨折,这种分型也能预测肱骨头血运。2018年发布的新版AO分型中也对肱骨近端骨折分型做出了更新,但是也没有提及内侧壁概念。RESCH等[26]通过描述肱骨近端骨折后肱骨头与肱骨干的相对位置进行分型,这种分型能判断受伤时暴力的作用方向,对于骨折的复位很重要,有文献也发现这种分型是所有分型中组间和组内差异性最低[29]。RESCH等[26]发现外翻嵌插骨折中,肱骨近端内侧铰链结构通常完整,而在内翻骨折中肱骨距区域通常骨折伴移位。这也可能解释了肱骨近端内翻骨折畸形中肱骨头缺血和继发性坏死发生率较高的原因。 2.3.4 外伤致肱骨距粉碎的机制 肱骨近端骨折作为“脆性骨折”,易发生在老年骨质疏松的患者。解剖上肱骨近端存在一个约130°的颈干角,30°后倾角,摔伤时应力直接传导到肱骨近端;或者肱骨距作为小结节向内的延续,小结节作为肩胛下肌的附着点,受到外力时肩胛下肌强烈收缩,引起小结节下后方骨折,导致肱骨距区域的骨折。 2.3.5 内侧壁的粉碎也可为医源性损伤 ①肱骨近端骨折也被称为“未被解决的骨折”,其处理比较困难的3大主要原因是:粉碎性骨折难以重建、骨质疏松难以维持复位、肱骨头坏死难以预测。粉碎肱骨近端骨折复位固定困难,临床医生术中对移位、嵌顿的肱骨头,用Joystick技术、撬拨复位时导致内侧壁粉碎。另外,也有部分医师术中操作暴力等直接导致内侧壁粉碎而不能重建。肱骨骨折钢板固定术后并发症报道不一,CAI等[22]报道并发症发生率为35%,并认为并发症部分归功于不正确的手术技术,由于复杂的肱骨近端骨折治疗学习曲线长,建议手术应该由有经验的外科医生进行。②医生对内侧壁重要性理解不够,只关注于主要骨折块(解剖矩、外科颈、大小结节)的复位过程,因而导致内侧壁复位不良或者内侧壁粉碎。或者医师没有正确把握切开复位内固定指征,对于内侧壁严重粉碎的不具备钢板内固定指征的骨折强行复位,进而加重内侧壁粉碎,这将引起严重后果。③常规钢板治疗肱骨近端骨折手术入路为胸大肌三角肌入路、劈三角肌外侧入路,但是此方法主要用于复位解剖颈、大结节、外科颈骨折,因为肱骨头存在30°后倾角及肩胛下肌的遮挡,肱骨距暴露相对较困难,因此不能很好的复位,这也是内侧壁复位不良甚至内侧壁医源性损伤的原因,所以有的学者提出可以行肩胛下肌剥离入路,这样可以直视下复位内侧壁[30]。④术中向薄弱的内侧壁打入螺钉时,锁定钢板型号与肱骨不匹配也会影响螺钉远端的位置,或钢板位置放置过于偏上或偏下致内侧壁骨折或粉碎;或术中为了固定对侧皮质,因螺钉的切割作用导致内侧壁粉碎。 2.4 累及肱骨距的肱骨近端骨折的钢板治疗 肱骨近端骨折治疗的方式很多,个体情况不同,治疗方式的选择也会不同,每种治疗方式都有其适应证、禁忌证,也都有优缺点[31-35],见表1。因此,如何选择最合适的治疗方式需要结合患者的年龄、身体情况、骨质情况、骨折类型、功能要求及手术者的经验综合判断。 "

对于严重的关节内骨折、关节周围骨折,如何“保头”并使患者有较好的临床效果是临床医师一直追求的,接骨板在肱骨近端骨折的保头治疗中的具有不可替代的作用并且也能获得不错的临床效果。既往认为钢板治疗肱骨近端骨折治疗的目的是恢复大结节、小结节解剖及关节面的平整,恢复并维持正常的颈干角,修复损伤的肩袖肌腱,使患者能进行早期功能锻炼,减少术后并发症的发生。但是越来越多的研究都证实获得内侧柱的支撑、内侧壁的解剖复位的重要性,近年的研究热点聚焦在肱骨近端骨折伴肱骨距粉碎的“保头治疗”及如何获得内侧柱支撑的方面。 2.4.1 Philos钢板结合下内侧螺钉(即距螺钉) Phillos钢板结合距螺钉使肱骨头能获有效支撑,减小螺钉和骨质接触面的应力,增强肱骨头固定的稳定性,可有效降低肱骨头内翻、螺钉穿出等并发症。GARDNER等[15]首次证明了内侧柱支撑与维持骨折复位之间的关系:通过解剖复位内侧壁和放置距螺钉,能显著减少内翻塌陷发生。而当内侧柱未获得有效支撑时,整个锁定钢板内固定系统需抵抗肩袖收缩产生的强大内翻应力,锁定螺钉和骨质接触面的应力增加,肱骨头内翻并发症则增加。近期一项纳入190例肱骨近端骨折患者随访至少3年的单中心研究也发现,与不使用下内侧螺钉相比,使用下内侧螺钉能显著降低术后内翻畸形发生率;若骨折内固定术后仍残留内翻畸形(复位不良),手术失败率则明显增加[36]。这也提示下内侧螺钉和解剖复位对肱骨近端骨折复位的重要性,体外研究同样证明内侧壁解剖复位和距螺钉内侧柱支撑的重要性。ZHANG等[37]体外生物力学研究发现采用2根距螺钉并保持内侧皮质骨接触,进行应力试验时强度最高,变形最小。而单纯下内侧皮质骨支撑比单独放置距螺钉具有更好的动态和静态生物力学性能,进一步说明内侧壁解剖复位在维持肱骨头稳定性上比使用距螺钉更好。但是在内侧壁粉碎,肱骨距无法获得解剖复位时,使用下内侧螺钉则能发挥一定抗内翻作用。目前肱骨近端骨折钢板固定时使用下内侧螺钉已达成共识,但是Philos钢板中锁定钉及下内侧螺钉的数量及位置仍然没有统一的观点,临床医生多是根据自己的经验置入螺钉。ERHARDT等[38]在尸体上研究认为在伴有内侧皮质粉碎骨折的患者中肱骨头内至少要置入5枚螺钉和1枚下方支撑螺钉,这样才能达到稳定的效果。而最新研究也表明,锁定钢板固定低骨密度肱骨近端不稳定骨折时,螺钉的构型对断钉失效风险有显著影响,有限元分析发现额外的螺钉使用减少螺钉周围的应变力,近端普通锁定螺钉之间的距离应尽可能大,且推荐对于不稳定肱骨近端骨折矩螺钉均应使用[39]。 对于肱骨近端内侧皮质完整时,使用距螺钉并获得肱骨距的解剖复位能获得较好的效果;而对于内侧粉碎的,特殊的距螺钉可以用来稳定内侧柱。同时临床上需要更多的研究来规定并规范螺钉的置入方式及数量。 2.4.2 钢板结合不同植骨支撑方式 肱骨近端骨折治疗一大困难是骨质疏松难以固定,因此通过植骨提高骨强度加强固定是可行的思路,植骨和骨替代材料是目前肱骨近端骨折内固定治疗中常用的加强固定方式。 钢板结合不同形式植骨:骨质疏松肱骨近端骨折患者,手术复位后肱骨近端内侧会出现较大的骨缺损,导致肱骨近端稳定性差。因此对于内侧肱骨距严重粉碎、内侧壁缺损或严重骨质疏松的患者,可以考虑植骨,目前最常用的植骨材料及方式是使用髓内同种异体腓骨结构性支撑植骨,将腓骨塑形插入肱骨近端髓腔中支撑肱骨头。植骨可以减少外侧置入螺钉的工作长度,辅助进行骨折间接复位、提供大量骨质加强螺钉钢板的固定强度,避免术后复位丢失。大量的临床研究也证明髓内同种异体腓骨移植治疗肱骨近端骨折具有较好的临床疗效[19,40-43]。 单纯Philos钢板治疗肱骨近端骨折,患者年龄越大,往往治疗后并发症高,治疗效果差。而髓内腓骨移植在治疗高龄患者时能取得不错的治疗效果,HINDS等[44]研究发现年龄大于65岁和小于65岁的肱骨近端骨折患者采用锁定钢板固定联合髓内异体腓骨移植治疗后,2组患者的临床结果比较差异无显著性意义。此外在治疗复杂粉碎性肱骨近端骨折时,尤其是四部分骨折,与钢板、关节置换相比,髓内腓骨移植也表现出更大的优势。KIM等[45]回顾性分析多中心164例老年肱骨三、四部分骨折的患者,分别行下内侧螺钉固定和腓骨移植,随访2年临床结果显示四部分骨折,腓骨移植组Constant评分、目测类比评分明显优于距螺钉组,且术后并发症明显低于距螺钉组,而在三部分骨折中2组差异无显著性意义。CHOW等[46]的生物力学实验也证实这点。而CHEN等[47]报道一项前瞻性病例对照研究,比较锁定钢板内固定联合髓内同种异体腓骨移植与半肩关节置换治疗骨质疏松性Neer四部分肱骨近端骨折的疗效,结果发现前者功能评分均显著高于后者,且术后并发症发生率低于后者。虽然有这么多优势,但是有学者提出腓骨髓内移植的术后若再发生肱骨头坏死等需要行关节置换时,则处理比较困难[48]。因此也有学者提出使用髂骨移植将结构性骨块紧贴内侧皮质放置来支撑粉碎的肱骨距以达到良好的内侧支撑。 因此,而对于内侧壁粉碎、大量骨缺损时单纯下内侧螺钉固定难以维持肱骨头稳定,此时行腓骨、髂骨移植,可减少内翻发生率。 骨水泥增强:肱骨近端髓内腓骨移植术后翻修困难,故有学者提出对于肱骨头粉碎、内侧皮质支撑丧失的三、四部分肱骨近端骨折,术前评估发现肱骨头坏死可能性大,不推荐使用髓内腓骨移植,可采用磷酸钙骨水泥加强固定,若肱骨头坏死再行关节置换手术。但是在行骨水泥注射时,必须保证对肱骨距进行复位以保证磷酸钙骨水泥不会渗透进入软组织。如果肱骨距过于粉碎无法复位,可以在透视下缓慢注入骨水泥,将注射套管针或者注射器针头远离内肱骨距,以防止骨髓内的扩散。 对于肱骨头粉碎、通过全面评估保肱骨头可能性很大时,可先考虑行骨水泥增强固定,后期发生坏死再行关节置换翻修。 2.4.3 内外侧双钢板 肱骨内侧柱未获得有效支撑后会导致内翻畸形、螺钉穿出等并发症,对于伴肱骨距粉碎的肱骨近端骨折,有的学者提出同时使用内侧支撑钢板固定,这种方法直接对内侧柱和外侧柱进行固定,理论上能取得更好的效果。PARK等[49]报道了17例采用内外侧双钢板治疗肱骨近端骨折伴内侧柱不稳定的患者,所有患者骨折均愈合,术后无内翻畸形、螺钉穿出等并发症发生。HE等[50]体外生物力学研究比较单纯锁定钢板、内侧解剖锁定钢板结合锁定钢板、腓骨移植结合锁定钢板、锁定钢板结合桡骨远端钢板治疗肱骨距粉碎的肱骨近端骨折模型,通过有限元分析发现内外侧双锁定钢板组在整体和局部结构刚度明显高于其他3种固定方法,且承受的等效应力最小,内侧解剖锁定钢板的使用能分散外侧锁定板上的应力,且颈干角变化最小。内侧钢板的使用目前局限在生物力学研究,临床研究较少,根据AO内固定使用原则:内固定物不放在应力侧、尽量减少对血运的破坏,而内侧支撑钢板正好与这相悖,这可能是肱骨近端骨折内侧钢板不能临床推广的原因。 所有这些固定方式最终的目的都是为了重建粉碎的肱骨距,恢复内侧柱的稳定,维持肱骨头的稳定,最终减少术后内翻畸形、螺钉穿出关节面等并发症。 2.5 肩袖修复对内侧壁支撑也是至关重要的 肱骨近端骨折,尤其是内侧壁粉碎时,常常合并肩袖损伤,肱骨内侧为应力侧,外侧作为张力侧,肩袖收缩能使肱骨头产生内翻趋势,肩袖产生的内翻牵拉应力以及合并的肱骨距粉碎会共同导致内翻塌陷和治疗失败。避免出现内翻塌陷的措施包括中和肩袖的拉力,修复重建肱骨距。可以使用粗的不可吸收编织缝线将肌腱缝合捆绑在钢板上,该方法可以将肩袖产生的拉力直接传导至钢板,使肩袖牵拉产生的张力与内侧柱支撑应力达到平衡。 2.6 预防措施 肱骨近端骨折术后并发症的发生被认为与肱骨距粉碎情况或复位情况相关,而目前研究热点是如何通过加强内侧支撑防止肱骨头塌陷等并发症,临床预防也是患者取得较好功能的关键一步。在临床实践中,需要系统评估可能导致肱骨近端骨折术后出现一系列并发症的危险因素,主要从以下几个方面来评估:①术前充分考虑患者年龄、性别等基本情况,术前完善相关影像学检查,了解患者的骨折情况,包括骨折分型及肱骨距情况,根据肱骨距的骨折模式,制定合理的手术方案,并进行良好的术前设计。②手术应该由高年资有经验医师进行,术者需要加强对肱骨距的重要性的认识,术中操作谨慎,避免暴力复位等操作,尽量解剖复位恢复内侧柱支撑。尽量应用距撑螺钉,以保证骨折的稳定并支撑肱骨头,肱骨距螺钉置于的位置应在肱骨头内下象限,靠近内侧皮质。③可适当加入磷酸盐骨水泥及自体移植腓骨来加强骨折薄弱区,从而进一步加强对肱骨头的支撑作用。④术中修复伴随的肩袖损伤、术后正确的指导患者功能锻炼。⑤密切功能随访,随访时间最少5年[51]。 "

| [1] PALVANEN M, KANNUS P, NIEMI S, et al. Update in the epidemiology of proximal humeral fractures. Clin Orthop Relat Res. 2006;442:87-92. [2] BEERES FJP, HALLENSLEBEN NDL, RHEMREV SJ, et al. Plate fixation of the proximal humerus: an international multicentre comparative study of postoperative complications. Arch Orthop Trauma Surg. 2017;137(12):1685-1692. [3] HAASTERS F, SIEBENBURGER G, HELFEN T, et al. Complications of locked plating for proximal humeral fractures-are we getting any better? J Shoulder Elbow Surg. 2016;25:e295-e303. [4] HASAN AP, PHADNIS J, JAARSMA RL, et al.Fracture line morphology of complex proximal humeral fractures .J Shoulder Elbow Surg .2017; 26(10):e300-e308. [5] RUSSO R, CAUTIERO F, DELLA ROTONDA G.The classification of complex 4-part humeral fractures revisited: the missing fifth fragment and indications for surgery .Musculoskelet Surg. 2012;96 Suppl 1: S13-19. [6] HERTEL R, HEMPFING A, STIEHLER M, et al. Predictors of humeral head isehemia after intracapsular fracture of the proximal humerus. J Shoulder Elbow Surg. 2004;13(4):427-433. [7] OSTERHOFF G, HOCH A, WANNER GA, et al.Calcar comminution as prognostic factor of clinical outcome after locking plate fixation of proximal humeral fractures. Injury.2012;10:1651-1656. [8] MAJED A, THANGARAJAH T, SOUTHGATE D, et al. Cortical thickness analysis of the proximal humerus.Shoulder Elbow. 2019; 11(2):87-93. [9] LEE SY, KWON SS, KIM TH, et al. Is central skeleton bone quality a predictor of the severity of proximal humeral fractures? Injury. 2016; 47(12):2777-2782. [10] 王烨明,李健,杨建华,等.肱骨近端内侧柱的解剖学测量研究[J].中华医学杂志,2018,98(39):3187-3191. [11] HETTRICH CM, BORAIAH S, DYKE JP, et al. Quantitative assessment of the vascularity of the proximal part of the humerus.J Bone Ioint Surg Am.2010;92(4):943-948. [12] KRALINGER F, UNGER S, WAMBACHER M, et al. The medial periosteal hinge, a key structure in fractures of the proximal humerus: a biomechanical cadaver study of its mechanical properties.. J Bone Joint Surg Am.2009;91(7):973-976. [13] 冷昆鹏,王艳华,陈建海,等.肱骨近端三维有限元模型的建立与生物力学分析[J].中国创伤骨科杂志,2015,17(4):326-330. [14] AGUDELO J, SCHURMANN M, STAHEL P, et al.Analysis of efficacy and failure in proximal humerus fractures treated with locking plates.J Orthop Trauma.2007;21(10):676-681. [15] GARDNER MJ, WEIL Y, BARKER JU,et al.The importance of medial support in locked plating of proximal humerus fractures.J Orthop Trauma.2007;21(3):185-191. [16] PONCE BA, THOMPSON KJ, RAGHAVA P, et al.The role of medial comminution and calcar restoration in varus collapse of proximal humeral fractures treated with locking plates.J Bone Joint Surg Am. 2013;95(16):e113. [17] GARDNER MJ, BORAIAH S, HELFET DL, et al.Indirect medial reduction and strut support of proximal humerus fractures using an endosteal implant.J Orthop Trauma. 2008;22(3):195-200. [18] JUNG SW, SHIM SB, KIM HM, et al.Factors that influence reduction loss in proximal humems fracture surgery. J Orthop Trauma.2015; 29(6):276-282. [19] MATASSI F, ANGELONI R, CARULLI C, et al. Locking plate and fibular allograft augmentation in unstable fractures of proximal humerus. Injury. 2012;43(11):1939-1942. [20] TRIKHA V,SINGH V,CHOUDHURY B,et al.Retrospective analysis of proximal humeral fracture-dislocations managed with locked plates. J Shoulder Elbow Surg. 2017;26(10):e293-299. [21] CAMPOCHIARO G, REBUZZI M, BAUDI P, et al. Complex proximal humerus fractures: Hertel's criteria reliability to predict head necrosis. Musculoskelet Surg.2015;99(Suppl 1):9-15. [22] CAI P, YANG Y, XU Z, et al. Anatomic locking plates for complex proximal humeral fractures: anatomic neck fractures versus surgical neck fractures.J Shoulder Elbow Surg. 2019;28(3):476-482. [23] BRUNNER F, SOMMER C, BAHRS C, et al. Open reduction and internal fixation of proximal humerus fractures using a proximal humeral locked plate:a prospective multicenter analysis. J Orthop Trauma. 2009;23(3):163-172. [24] HELWIG P, BAHRS C, EPPLE B, et al. Does fixed-angle plate osteosynthesis solve the problems of a fractured proximal humerus?A prospective series of 87 patients. Acta Orthop. 2009;80(1):92-96. [25] CHEN H, JI X, ZHANG Q, et al.Clinical outcomes of allograft with locking compression plates for elderly four-part proximal humerus fractures. J Orthop Surg Res. 2015;10:114. [26] RESCH H, TAUBER M, NEVIASER RJ, et al.Classification of proximal humeral fractures based on a pathomorphologic analysis .J Shoulder Elbow Surg .2016 ;25(3):455-462. [27] MEINBERG EG, AGEL J, ROBERTS CS, et al. Fracture and dislocation classification compendium-2018. J Orthop Trauma.2018;32 Suppl 1:S1-S170. [28] KHANNA K, BRABSTON EW, QAYYUM U, et al. Proximal humerus fracture 3-D modeling. Am J Orthop (Belle Mead NJ). 2018;47(4). doi: 10.12788/ajo.2018.0023. [29] MAJED A, MACLEOD I, BULL AM, et al.Proximal humeral fracture classification systems revisited. J Shoulder Elbow Surg. 2011;20(7): 1125-1132. [30] CHERNEY SM, MURPHY RA, ACHOR TS, et al. Subscapularis peel for open reduction and internal fixation of proximal humerus fractures with a head split. J Orthop Trauma. 2018;32(12):e487-e491. [31] SUN Q, GE W, LI G, et al.Locking plates versus intramedullary nails in the management of displaced proximal humeral fractures:a systematic review and meta-ananlysis. Int Orthop. 2018;42(3):641-650. [32] SHI X, LIU H, XING R, et al. Effect of intramedullary nail and locking plate in the treatment of proximal humerus fracture: an update systematic review and meta-analysis. J Orthop Surg Res. 2019;14(1): 285. [33] GRUBHOFER F, WIESER K, MEYER DC, et al. Reverse total shoulder arthro- plasty for acute head-splitting, 3- and 4-part fractures of the proximal humerus in the elderly. J shoulder Elbow Surg. 2016; 25:1690-1698. [34] VAN DER MERWE M, BOYLE MJ, FRAMPTON CMA, et al. Reverse shoulder arthroplasty compared with hemiarthroplasty in the treatment of acute proximal humeral fractures.J Shoulder Elbow Surg. 2017; 26(9):1539-1545. [35] REUTHER F, PETERMANN M, STANGL R. Reverse shoulder arthroplasty in acute fractures of the proximal humerus: Does tuberosity healing improve clinical outcomes? J Orthop Trauma. 2019;33:e46-51. [36] OPPEBØEN S, WIKERØY AKB, FUGLESANG HFS, et al. Calcar screws and adequate reduction reduced the risk of fixation failure in proximal humeral fractures treated with a locking plate: 190 patients followed for a mean of 3 years. J Orthop Surg Res. 2018;13(1):197. [37] ZHANG X, HUANG J, ZHAO L, et al. Inferomedial cortical bone contact and fixation with calcar screws on the dynamic and static mechanical stability of proximal humerus fractures. J Orthop Surg Res. 2019;14(1):1. [38] ERHARDT JB, STOFFEL K, KAMPSHOFF J, et al .The position and number of screws influence screw perforation of the humeral head in modern locking plates: a cadaver study. J Orthop Trauma. 2012;26(10): e188-192. [39] FLETCHER JWA, WINDOLF M, RICHARDS RG,et al.Screw configuration in proximal humerus plating has a significant impact on fixation failure risk predicted by finite element models. J Shoulder Elbow Surg. 2019;28(9):1816-1823. [40] LITTLE MT, BERKES MB, SCHOTTEL PC, et al. The impact of preoperative coronal plane deformity on proximal humerus fixation with endosteal augmentation. J Orthop Trauma. J Orthop Trauma. 2014;28(6):338-347. [41] NEVIASER AS, HETTRICH CM, BEAMER BS, et al. Endosteal strut augment reduces complications associated with proximal humeral locking plates. Clin Orthop Relat Res. 2011;469(12):3300-3306. [42] TAN E, LIE D, WONG MK. Early outcomes of proximal humerus fracture fixation with locking plate and intramedullary fibular strut graft. Orthopedics. 2014;37(9):e822-827. [43] HSIAO CK, TSAI YJ, YEN CY, et al.Intramedullary cortical bone strut improves the cyclic stability of osteoporotic proximal humeral fractures. BMC Musculoskelet Disord. 2017;18(1):64. [44] HINDS RM, GARNER MR, TRAN WH, et al.Geriatric proximal humeral fracture patients show similar clinical outcomes to non-geriatric patients after osteosynthesis with endosteal fibular strut allograft. J Shoulder Elbow Surg. 2015;24(6):889-896. [45] KIM DS, LEE DH, CHUN YM, et al. Which additional argmented fixation procedure decreases suigical failure after proximal humeral fracture with medial comminution :fibular allograft or infermedial screws? J Shoulder Elbow Surg. 2018;27(10):1852-1858. [46] CHOW RM, BEGUM F, BEAUPRE LA, et al.Proximal humeral fracture fixation: locking plate construct ± intramedullary fibularallograft.J Shoulder Elbow Surg. 2012;21(7):894-901. [47] CHEN H, JI X, GAO Y, et al.Comparison of intramedullary fibular allograft with locking compression plate versus shoulder hemiarthroplasty for repair of osteoporotic four-part proximal humerus fracture:Consecutive,prospective,controlled,and comparative study. Orthop Traumato Surg Res. 2016;102(3):287-292. [48] AMINI MH.Managing the endosteal fibula during arthroplasty for proximal humeral fracture sequelae.J Orthop Trauma. 2019;33 Suppl 1:S1-S2. [49] PARK SG, KO YJ. Medial buttress plating for humerus fractures with unstable medial column. J Orthop Trauma. 2019;33(9):352-359. [50] HE Y, ZHANG Y, WANG Y, et al .Biomechanical evaluation of a novel dualplate fixation method for proximal humeral fractures without medial support. J Orthop Surg Res. 2017;12(1):72. [51] ZIRNGIBL B, BIBER R, BAIL HJ.Humeral head necrosis after proximal humeral nailing: what are the reasons for bad outcomes? Injury. 2016; 47 Suppl 7:S10-S13. |
| [1] | Zhang Shangpu, Ju Xiaodong, Song Hengyi, Dong Zhi, Wang Chen, Sun Guodong. Arthroscopic suture bridge technique with suture anchor in the treatment of acromioclavicular dislocation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1417-1422. |
| [2] | Hu Kai, Qiao Xiaohong, Zhang Yonghong, Wang Dong, Qin Sihe. Treatment of displaced intra-articular calcaneal fractures with cannulated screws and plates: a meta-analysis of 15 randomized controlled trials [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1465-1470. |
| [3] | Jiang Hongying, Zhu Liang, Yu Xi, Huang Jing, Xiang Xiaona, Lan Zhengyan, He Hongchen. Effect of platelet-rich plasma on pressure ulcers after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1149-1153. |
| [4] | Li Cai, Zhao Ting, Tan Ge, Zheng Yulin, Zhang Ruonan, Wu Yan, Tang Junming. Platelet-derived growth factor-BB promotes proliferation, differentiation and migration of skeletal muscle myoblast [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1050-1055. |
| [5] | Xu Yulin, Shen Shi, Zhuo Naiqiang, Yang Huilin, Yang Chao, Li Yang, Zhao Heng, Zhao Lu. Biomechanical comparison of three different plate fixation methods for acetabular posterior column fractures in standing and sitting positions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 826-830. |
| [6] | He Li, Tian Wei, Xu Song, Zhao Xiaoyu, Miao Jun, Jia Jian. Factors influencing the efficacy of lumbopelvic internal fixation in the treatment of traumatic spinopelvic dissociation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 884-889. |
| [7] | Yang Weiqiang, Ding Tong, Yang Weike, Jiang Zhengang. Combined variable stress plate internal fixation affects changes of bone histiocyte function and bone mineral density at the fractured end of goat femur [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 890-894. |
| [8] | Kong Lingbao, Lü Xin. Effect of implant selection and approach on support in the operation of posterolateral tibial plateau fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 942-947. |
| [9] | He Xiangzhong, Chen Haiyun, Liu Jun, Lü Yang, Pan Jianke, Yang Wenbin, He Jingwen, Huang Junhan. Platelet-rich plasma combined with microfracture versus microfracture in the treatment of knee cartilage lesions: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 964-969. |
| [10] | Xu Junma, Yu Yuechao, Liu Zhi, Liu Yu, Wang Feitong. Application of 3D-printed coplanar template combined with fixed needle technique in percutaneous accurate biopsy of small pulmonary nodules [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 761-764. |
| [11] | Liu Jiangfeng. Nano-hydroxyapatite/polyamide 66 composite filling combined with locking plate in the treatment of fibrous dysplasia of femoral bone [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 542-547. |
| [12] | Xu Jianxia, Wang Zhaoxu, Wang Chunren. Blood compatibility of disposable blood perfusion device in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 588-592. |
| [13] | Li Yang, Zhang Mingyong. Meta-analysis of the effect of double Endobutton and clavicular hook plate on the treatment of acromioclavicular dislocation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 463-470. |
| [14] | Li Yanle, Yue Xiaohua, Wang Pei, Nie Weizhi, Zhang Junwei, Tan Yonghai, Jiang Hongjiang. Intramedullary nail fixation versus plate fixation in the treatment of displaced midshaft clavicular fractures in adults: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 471-476. |
| [15] | Jiang Tao, Ma Lei, Li Zhiqiang, Shou Xi, Duan Mingjun, Wu Shuo, Ma Chuang, Wei Qin. Platelet-derived growth factor BB induces bone marrow mesenchymal stem cells to differentiate into vascular endothelial cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3937-3942. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||